Applicazione legge della termodinamica generalizzata
Ciao a tutti,
sto seguendo le lezioni di Fisica I del prof. Rasetti su Uninettuno. L'approccio che usa è basato sulla termodinamica generalizzata e sulla legge generale di Gibbs per l'energia (in particolare l'entropia ha un termine di sorgente sempre positivo, ovvero non puo' essere mai annichilita).
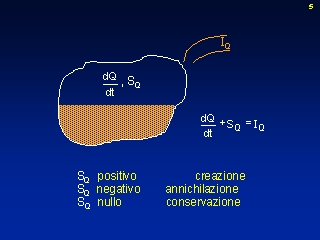
Nel seguito viene proposto questo esempio (espansione libera):
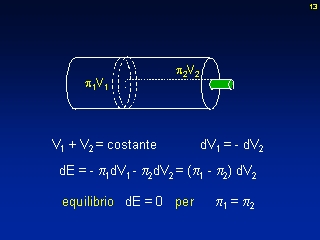
con il seguente commento: "L’esempio trattato mostra il raggiungimento dell’equilibrio secondo la regola di energia minima quando le pressioni sono divenute uguali. Durante il processo naturale di raggiungimento dell’equilibrio il volume “passa” dalle pressioni più alte a quelle più basse. Muovendo invece il pistone dall’esterno si realizza il processo inverso, il passaggio di volume dalle pressioni più basse a quelle più alte. L’esempio sottolinea la natura di scambio di questa forma di energia; in altre parole l’Energia di Compressione o Espansione come tale non può essere contenuta nel SF ma solamente scambiata: è una grandezza di Processo e non di Stato e quindi per essere trattenuta tale energia deve cambiare portatore".
Da quanto capisco, qui il volume "passa" dalla regione 1 alla regione 2 in quanto $dV_1$ è negativo e $dV_2$ è positivo (nell'esempio la pressione $\pi_2 > \pi_1$). Rasetti dice che in generale i processi spontanei sono sempre nella direzione in cui una "grandezza estensiva di tipo quantità..." (in questo caso il volume) passa da un regione con potenziale (qui la grandezza intensiva pressione) maggiore ad una a potenziale minore.
Il ragionamento mi torna se le pressioni $\pi$ sono in realtà considerate con il segno negativo, questo in linea con l'espressione per la variazione di energia del sistema dovuta alle pressioni/volumi $dE = - \pi dV$.
Come la vedete ? Grazie.
sto seguendo le lezioni di Fisica I del prof. Rasetti su Uninettuno. L'approccio che usa è basato sulla termodinamica generalizzata e sulla legge generale di Gibbs per l'energia (in particolare l'entropia ha un termine di sorgente sempre positivo, ovvero non puo' essere mai annichilita).

Nel seguito viene proposto questo esempio (espansione libera):

con il seguente commento: "L’esempio trattato mostra il raggiungimento dell’equilibrio secondo la regola di energia minima quando le pressioni sono divenute uguali. Durante il processo naturale di raggiungimento dell’equilibrio il volume “passa” dalle pressioni più alte a quelle più basse. Muovendo invece il pistone dall’esterno si realizza il processo inverso, il passaggio di volume dalle pressioni più basse a quelle più alte. L’esempio sottolinea la natura di scambio di questa forma di energia; in altre parole l’Energia di Compressione o Espansione come tale non può essere contenuta nel SF ma solamente scambiata: è una grandezza di Processo e non di Stato e quindi per essere trattenuta tale energia deve cambiare portatore".
Da quanto capisco, qui il volume "passa" dalla regione 1 alla regione 2 in quanto $dV_1$ è negativo e $dV_2$ è positivo (nell'esempio la pressione $\pi_2 > \pi_1$). Rasetti dice che in generale i processi spontanei sono sempre nella direzione in cui una "grandezza estensiva di tipo quantità..." (in questo caso il volume) passa da un regione con potenziale (qui la grandezza intensiva pressione) maggiore ad una a potenziale minore.
Il ragionamento mi torna se le pressioni $\pi$ sono in realtà considerate con il segno negativo, questo in linea con l'espressione per la variazione di energia del sistema dovuta alle pressioni/volumi $dE = - \pi dV$.
Come la vedete ? Grazie.
Risposte
Credo tu ti stia dimenticando che, in quella formula, ti ritrovi con la differenza tra le pressioni (che quindi può essere sia positiva che negativa).
L'equilibrio è raggiunto quando l'energia potenziale termodinamica ha un minimo (come per l'energia potenziale meccanica), ma per determinare il potenziale termodinamico da minimizzare è necessario definire le condizioni al contorno.
Se il sistema ha V totale costante, il potenziale da minimizzare è quello di Helmholtz
Se il sistema è termostatato allora dT=0 e quindi
ovvero
avendo scelto come variabile V1 e poichè V2 = Vtot - V1, risulterà dV2=-dV1 e quindi
Imponendo che l'equilibrio sia un punto critico la derivata si deve annullare e quindi
Questo significa che se ci si discosta dal punto di minimo, dove le pressioni sono uguali, sia nel senso di aumentare V1 che di diminuirlo il potenziale aumenterà.
Infatti, come indicato da apatriarca, conta la differenza di pressione che sarà positiva per dV1>0 (diminuisce P1 e aumenta P2) e negativa per dV1<0 (aumenta P1 e diminuisce P2), per cui in entrambi i casi dF>0 ovvero F aumenta.
Se il sistema ha V totale costante, il potenziale da minimizzare è quello di Helmholtz
[math]dF = -SdT - PdV[/math]
Se il sistema è termostatato allora dT=0 e quindi
[math]dF = dF_1 + dF_2 = - P_1 dV_1 - P_2 dV_2[/math]
ovvero
[math]dF/dV_1 = -P_1 - P_2 dV_2/dV_1[/math]
avendo scelto come variabile V1 e poichè V2 = Vtot - V1, risulterà dV2=-dV1 e quindi
[math]dF/dV_1 = -P_1 + P_2[/math]
Imponendo che l'equilibrio sia un punto critico la derivata si deve annullare e quindi
[math]P_2 = P_1[/math]
Questo significa che se ci si discosta dal punto di minimo, dove le pressioni sono uguali, sia nel senso di aumentare V1 che di diminuirlo il potenziale aumenterà.
Infatti, come indicato da apatriarca, conta la differenza di pressione che sarà positiva per dV1>0 (diminuisce P1 e aumenta P2) e negativa per dV1<0 (aumenta P1 e diminuisce P2), per cui in entrambi i casi dF>0 ovvero F aumenta.


 Accedi a tutti gli appunti
Accedi a tutti gli appunti
 Tutor AI: studia meglio e in meno tempo
Tutor AI: studia meglio e in meno tempo